Autor de Applet: Curso Física por Ordenador del autor: Profesor Ángel Franco García, de la Escuela Universitaria de Ingeniería Técnica Industrial de Eibar, España.
Se define ciclo de Carnot como un proceso cíclico reversible que utiliza un gas perfecto, y que consta de dos transformaciones isotérmicas y dos adiabáticas, tal como se muestra en la figura.

La representación gráfica del ciclo de Carnot en un diagrama p-V es el siguiente
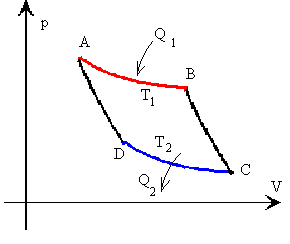 |
Tramo A-B isoterma a la temperatura T1
Tramo B-C adiabática Tramo C-D isoterma a la temperatura T2 Tramo D-A adiabática |
En cualquier ciclo, tenemos que obtener a partir de los datos iniciales:
- La presión, volumen de cada uno de los vértices.
- El trabajo, el calor y la variación de energía interna en cada una de los procesos.
- El trabajo total, el calor absorbido, el calor cedido, y el rendimiento del ciclo.
Los datos iniciales son los que figuran en la tabla adjunta. A partir de estos datos, hemos de rellenar los huecos de la tabla.
| Variables | A |
B |
C |
D |
| Presión p (atm) | pA | |||
| Volumen v (l) | vA | vB | ||
| Temperatura T (K) | T1 | T1 | T2 | T2 |
Las etapas del ciclo
Para obtener las variables y magnitudes desconocidas haremos uso de las fórmulas que figuran en el cuadro-resumen de las transformaciones termodinámicas.
- Transformación A->B (isoterma)
- Transformación B->C (adiabática)
- Transformación C->D (isoterma)
- Transformación D-> A (adiabática)
La presión pB se calcula a partir de la ecuación del gas ideal ![]()
Variación de energía interna ![]()
Trabajo ![]()
Calor ![]()
La ecuación de estado adiabática es ![]() o bien,
o bien, ![]() . Se despeja vc de la ecuación de la adiabática
. Se despeja vc de la ecuación de la adiabática ![]() . Conocido vc y T2 se obtiene pc, a partir de la ecuación del gas ideal.
. Conocido vc y T2 se obtiene pc, a partir de la ecuación del gas ideal. ![]() .
.
Calor ![]()
Variación de energía interna ![]()
Trabajo ![]()
Variación de energía interna ![]()
Trabajo ![]()
Calor ![]()
Se despeja vD de la ecuación de la adiabática
. Conocido vD y T2 se obtiene pD, a partir de la ecuación del gas ideal.
.
Calor
Variación de energía interna
Trabajo
El ciclo completo
- Variación de energía interna
En un proceso cíclico reversible la variación de energía interna es cero
- Trabajo
Los trabajos en las transformaciones adiabáticas son iguales y opuestos. A partir de las ecuaciones de las dos adiabáticas la relación entre los volúmenes de los vértices es
, lo que nos conduce a la expresión final para el trabajo.
- Calor
En la isoterma T1 se absorbe calor Q>0 ya que vB>vA de modo que

En la isoterma T2 se cede calor Q<0 ya que vD<vC
- Rendimiento del ciclo
Se define rendimiento como el cociente entre el trabajo realizado y el calor absorbido
Motor y frigorífico
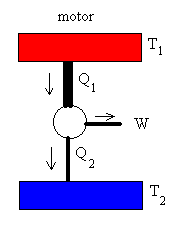 |
Un motor de Carnot es un dispositivo ideal que describe un ciclo de Carnot. Trabaja entre dos focos, tomando calor Q1 del foco caliente a la temperatura T1, produciendo un trabajo W, y cediendo un calor Q2 al foco frío a la temperatura T2.
En un motor real, el foco caliente está representado por la caldera de vapor que suministra el calor, el sistema cilindro-émbolo produce el trabajo, y se cede calor al foco frío que es la atmósfera. |
 |
La máquina de Carnot también puede funcionar en sentido inverso, denominándose entonces frigorífico. Se extraería calor Q2 del foco frío aplicando un trabajo W, y cedería Q1 al foco caliente.
En un frigorífico real, el motor conectado a la red eléctrica produce un trabajo que se emplea en extraer un calor del foco frío (la cavidad del frigorífico) y se cede calor al foco caliente, que es la atmósfera. |